Jalan Pintas Vaksin, Amankah?
Pemerintah harus berpikir jernih sebelum memutuskan apakah akan menggunakan vaksin lewat jalur cepat EUA dengan segala risikonya atau menunda program vaksin beberapa bulan dengan risiko lebih minimal dan terkontrol.

Presiden Joko Widodo memimpin rapat terbatas mengenai persiapan vaksin Covid-19 di Istana Merdeka, Jakarta, Senin (26/10/2020).
Pemerintah mengeluarkan pernyataan bahwa vaksin Covid-19 sudah akan tersedia pada November-Desember 2020 dan vaksinasi akan segera dimulai.
Hal ini disampaikan Menteri Koordinator Bidang Kemaritiman dan Investasi Luhut Binsar Pandjaitan, yang juga Wakil Ketua Penanganan Covid-19 dan Pemulihan Ekonomi Nasional.
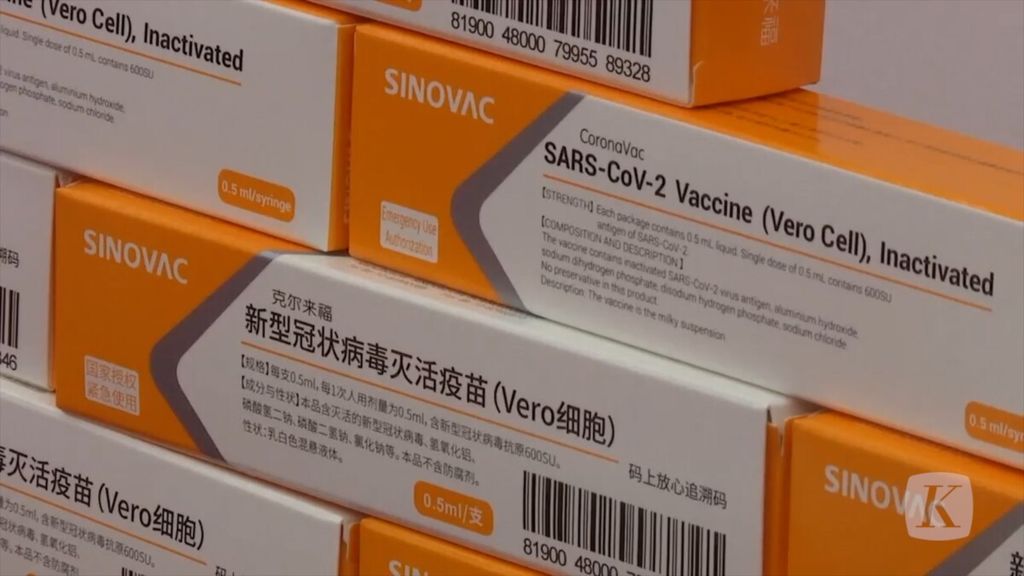
Pemerintah menargetkan akan memvaksinasi 100 juta penduduk pada Desember 2020-Januari 2021. Vaksin ini diharapkan diperoleh dari perusahaan G42 yang berbasis di Abu Dhabi sebanyak 30 juta unit dan sisanya dari perusahaan Sinovac, China.
Pada saat yang sama, Presiden Joko Widodo telah memerintahkan pembuatan segera rencana detail vaksinasi. Kementerian Kesehatan pun merespons. Direktorat Jenderal Pencegahan dan Pengendalian Penyakit (P2P) Kementerian Kesehatan telah membuat grand design/road map vaksinasi Covid-19 yang mencakup jumlah kebutuhan vaksin, sasaran, skema, dan target, termasuk pedoman teknis.
Baca juga: Tak Hanya Andalkan Vaksin
Dari gelagat itu, tampak bahwa program vaksinasi akan terealisasi. Namun, apakah realistis bahwa vaksinasi dapat berlangsung segera?
Dari gelagat itu, tampak bahwa program vaksinasi akan terealisasi.
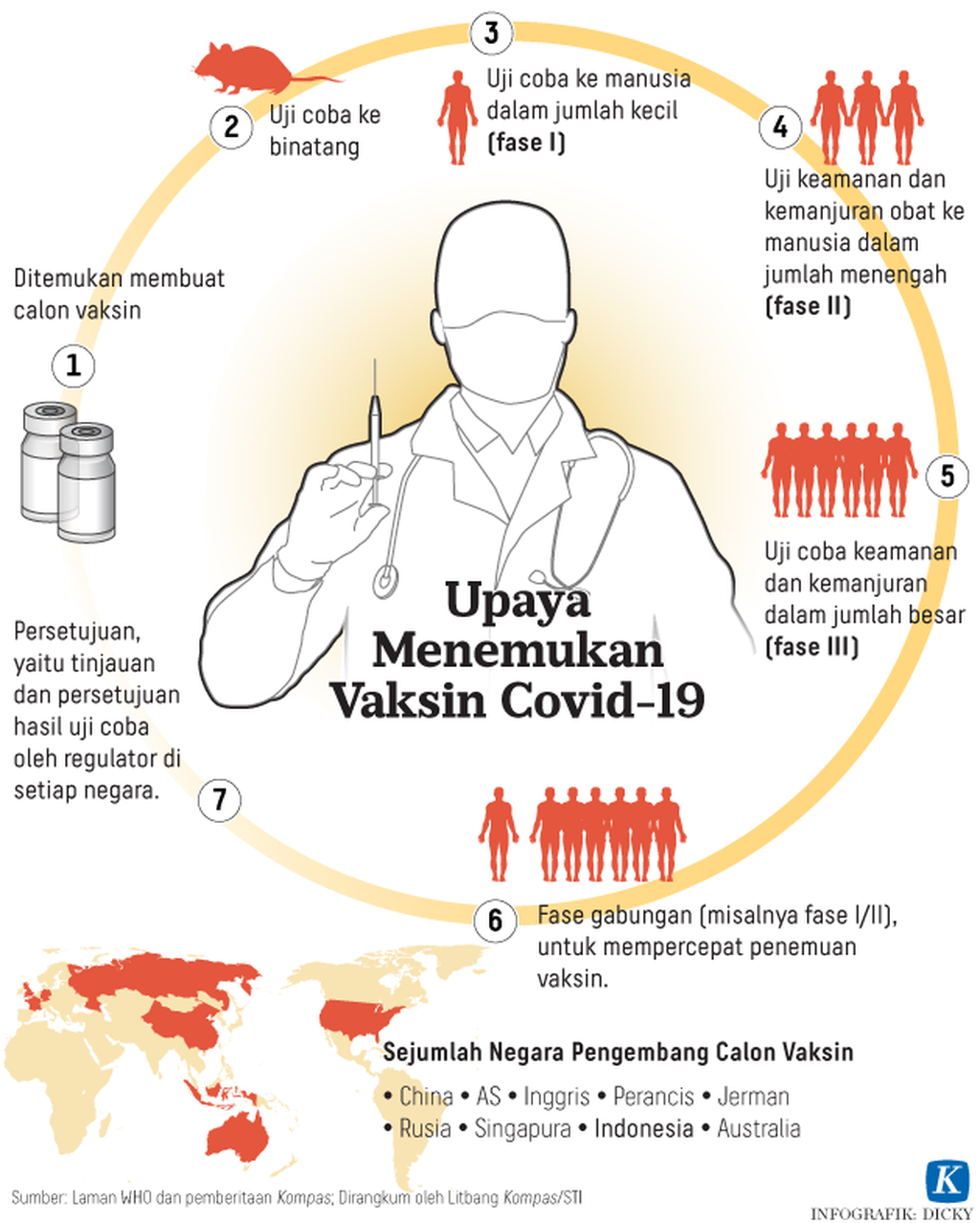
Uji vaksin
Semua kandidat vaksin Covid-19 harus menjalani uji efektivitas dan keamanan yang ketat. Ini untuk menjamin vaksin benar-benar aman dan efektif. Secara umum, uji ini meliputi uji pre-klinik, uji klinis tahap 1 hingga 3, serta post-marketing surveillance.
Proses pembuatan vaksin membutuhkan waktu rata-rata 10-15 tahun. Vaksin tercepat yang pernah diproduksi adalah vaksin mumps, yaitu empat tahun. Namun, karena pertimbangan kebutuhan mendesak, para ahli sepakat mempersingkat waktu uji vaksin Covid-19 menjadi 12-18 bulan saja.
Baca juga: Antisipasi Vaksin Covid-19
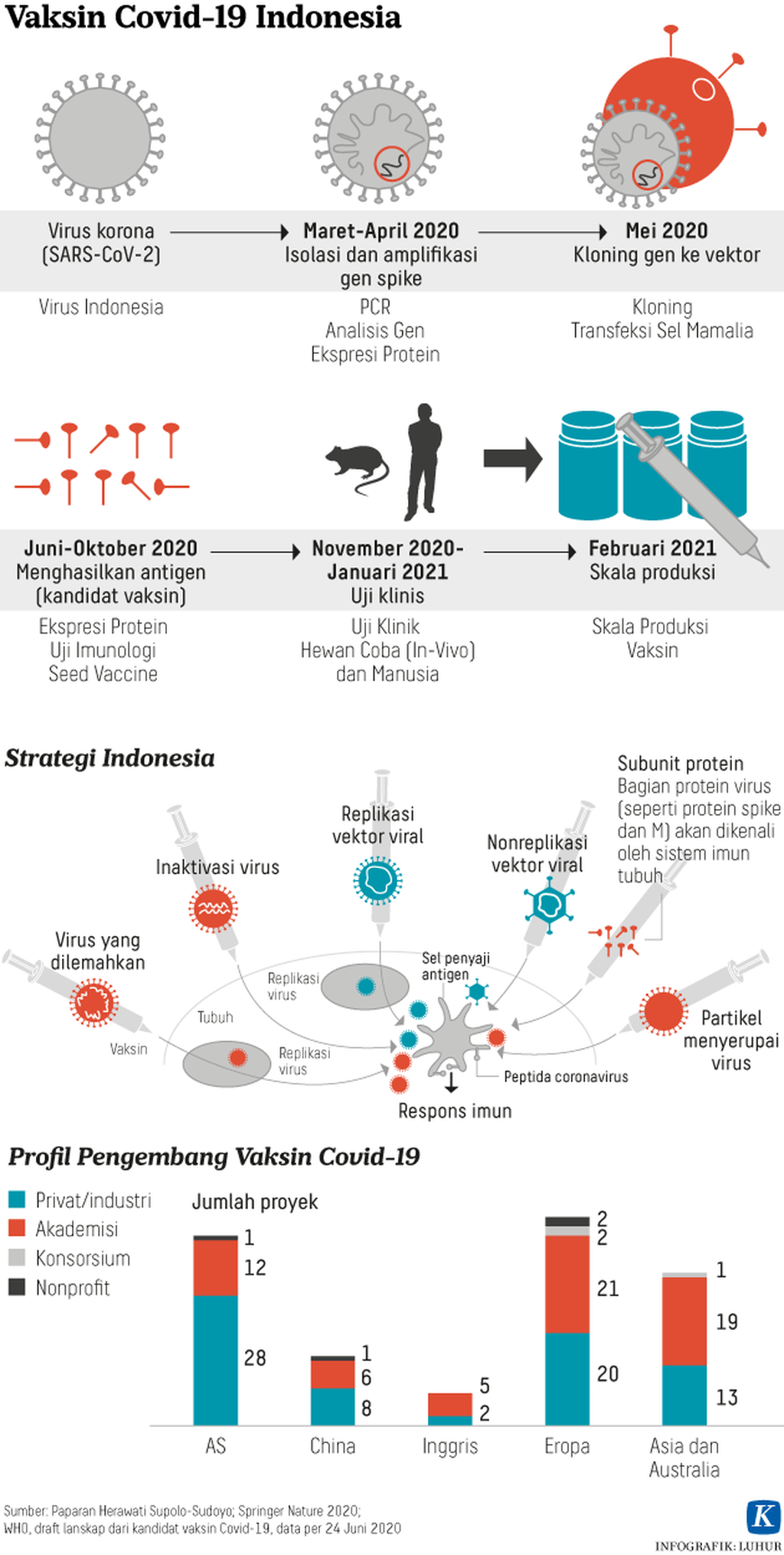
Saat ini, telah terdapat lebih dari 200 proyek vaksin di seluruh dunia. Dari jumlah itu, yang telah berada pada fase uji klinis sebanyak 31 proyek; delapan di antaranya telah berada pada fase 3 uji klinis. Artinya, dalam beberapa bulan mendatang, laporan uji klinis sejumlah vaksin telah dapat diketahui.
Pfizer mengklaim laporan uji klinis vaksinnya akan diserahkan akhir Oktober, sedangkan Moderna mengaku dapat melaporkan hasilnya pada akhir November. Namun, klaim kedua perusahaan vaksin ini diragukan sebagian ahli.
WHO sendiri mengestimasi bahwa laporan uji klinis vaksin baru akan diperoleh pada Desember 2020 atau Januari 2021. Setelah laporan diterima, regulatory approval body pada tiap negara akan mengkaji ulang laporan dan memberi keputusan penerimaan atau penolakan. Apabila disetujui, vaksin baru dapat diproduksi. Dengan proses ini, vaksin diharapkan dapat digunakan masyarakat pada pertengahan 2021.
Baca juga: Perlombaan Menciptakan Vaksin
Indonesia menjadi salah satu tempat uji klinis vaksin Sinovac. Saat ini terdapat sekitar 1.200 orang yang berpartisipasi dalam uji coba ini. Sekitar 400 orang di antaranya telah memperoleh vaksinasi kedua dan selanjutnya menjalani pemeriksaan darah untuk penentuan tingkat keamanan vaksin. Laporan keamanannya akan diperoleh pada akhir Januari 2021, sedangkan tingkat daya guna atau efikasi (efficacy)-nya baru dapat dilaporkan pada Maret 2021.
Indonesia menjadi salah satu tempat uji klinik vaksin Sinovac.
Apabila laporan keamanan dan efikasi ini disetujui, dibutuhkan waktu beberapa bulan bagi Biofarma memproduksi vaksin ini. Ini belum termasuk distribusi dan pelaksanaan vaksinasi.
Baca juga: Bio Farma Jadi Tempat Produksi 100 Juta Vaksin CEPI
Jika menggunakan jalur normal itu, kecil kemungkinan vaksinasi dapat dilakukan Desember ini.
”Emergency use authorization”
Selain jalur normal, sejumlah negara menggunakan jalur fast-track dalam proses uji coba dan produksi vaksin Covid-19. Jalur pintas ini disebut sebagai emergency use authorization (EUA), yaitu persetujuan cepat yang didasarkan pada kepentingan mendesak.
EUA merupakan izin atau persetujuan istimewa. Berdasarkan adanya kondisi kedaruratan dan krisis, persetujuan dapat diberikan kepada obat, zat, atau alat-alat medis tertentu sekalipun bahan-bahan tersebut belum melewati secara lengkap uji standar. Tujuannya adalah tersedianya secara cepat bahan untuk penanggulangan krisis.
Di Amerika, Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) diberi kesempatan menggunakan prinsip ini apabila terjadi kedaruratan kesehatan masyarakat.
Baca juga: Mendesain Vaksin Covid-19
/https%3A%2F%2Fkompas.id%2Fwp-content%2Fuploads%2F2020%2F08%2F20200811_ENGLISH-VAKSIN-COVID-19_C_web_1597157983.jpg)
Tim riset uji klinis calon vaksin Covid-19 menyimulasikan penyuntikan vaksin produksi Sinovac, China, kepada sukarelawan di gedung Fakultas Kedokteran Universitas Padjadjaran, Kota Bandung, Jawa Barat, Kamis (6/8/2020). Sebelum disuntik vaksin, calon sukarelawan akan menjalani pemeriksaan kesehatan, Selasa (11/8/2020).
Untuk hal ini, tiga kriteria yang harus terpenuhi adalah adanya ancaman serius dan besar terhadap kesehatan masyarakat, seperti kematian; terdapatnya bukti ilmiah bahwa bahan yang akan disetujui bersifat efektif dan punya lebih banyak keuntungan daripada kerugian, serta belum ada alternatif bahan yang dapat digunakan untuk mengatasi ancaman serius penyakit. Jika ketiga prinsip itu terpenuhi, sponsor dapat mengajukan usulan EUA untuk bahannya.
Di Amerika, sudah cukup banyak bahan yang disetujui lewat pintu EUA ini. Berbagai produk medis, seperti ventilator, APD, tes serologik, dan obat remdesivir, telah disetujui lewat EUA. Bahkan, obat antimalaria hydroxycholoroquin dan choloroquin juga mendapatkan persetujuan sebagai obat Covid-19 lewat EUA meski akhirnya persetujuan ini dicabut setelah berbagai studi melaporkan efek samping serius obat ini.
Salah satu bahan yang dapat memperoleh persetujuan EUA adalah vaksin Covid-19. Meski belum ada vaksin Covid-19 yang disetujui lewat EUA, FDA mengisyaratkan bahwa vaksin yang telah berada pada fase 3 dapat dipertimbangkan memperoleh EUA.
Salah satu bahan yang dapat memperoleh persetujuan EUA adalah vaksin Covid-19.
China dan Rusia malah sejak lama telah memberikan persetujuan EUA terhadap vaksin Covid-19-nya. Vaksin CanSino China telah mendapatkan persetujuan untuk digunakan di kalangan militer sejak Juni 2020, sedangkan vaksin Sputnik-V Rusia disetujui penggunaannya pada Agustus 2020.
Kedua vaksin disetujui bahkan sebelum vaksin ini memasuki uji klinis tahap 3. Di Uni Emirat Arab, vaksin Covid-19 dari Sinopharm juga baru-baru ini mendapatkan persetujuan EUA untuk digunakan bagi tenaga kesehatan.
Pro-kontra
Dalam sejumlah pernyataan, pemerintah mengisyaratkan akan menggunakan jalan pintas penyediaan vaksin, yaitu via pintu EUA. Artinya, pemerintah tak menunggu sampai seluruh fase uji klinis terlewati. Pemerintah kemungkinan akan berkoordinasi dengan Badan Pengawas Obat dan Makanan (BPOM) untuk dapat status EUA bagi vaksin yang akan diimpor dari China dan Abu Dhabi.
Baca juga: Jangan Terlena Euforia Vaksin
Meski pemerintah memiliki pengaruh kuat untuk memperoleh status EUA, banyak kondisi yang harus dipertimbangkan sungguh-sungguh. Pertama, vaksin yang belum melewati fase uji klinis lengkap, tingkat keamanannya belum terkonfirmasi.
Salah satu tujuan uji klinis fase 3, misalnya, adalah untuk mendeteksi adanya efek samping yang mungkin timbul pada satu dari beberapa ribu orang penerima vaksin. Jika fase ini tidak dilewati, efek samping yang tampak ”langka” ini tidak akan terdeteksi. Padahal, ketika diekstrapolasi kepada populasi pengguna vaksin, efek samping yang tampak ”langka” ini dapat menjadi sangat banyak.
Baca juga: Vaksin Covid-19 Tiba November Ini
Katakanlah, karena tidak melewati fase 3, sebuah efek samping vaksin yang terjadi pada 1 dari 10.000 penerima tidak terdeteksi. Saat memberikan vaksinasi kepada 260 juta penduduk, efek samping ini baru akan muncul pada 260.000 orang penerima vaksin.
Jika fase ini tidak dilewati, efek samping yang tampak ”langka” ini tidak akan terdeteksi.
Kedua, jika tidak melewati semua fase uji klinis, efikasi vaksin sulit diekstrapolasi kepada masyarakat umum.
Pada uji klinis fase 3, uji coba dilakukan kepada populasi luas dengan berbagai jenis umur, etnis, dan kondisi kesehatan. Ini berbeda dengan uji klinis fase 1 dan 2 yang lebih banyak dilakukan kepada orang sehat.
Artinya, tanpa melewati fase 3, sulit dikatakan bahwa vaksin terkonfirmasi efektif untuk semua jenis populasi, termasuk orang berusia di atas 55 tahun dan memiliki komorbiditas, yang merupakan kelompok risiko tinggi Covid-19. Memberikan vaksin yang efikasinya belum terkonfirmasi berpotensi menimbulkan pengendalian semu (pseudo-control).
Ketiga, di berbagai negara yang meloloskan vaksin lewat pintu EUA, vaksin diberikan hanya kepada kelompok populasi tertentu dengan jumlah terbatas. Di antaranya, hanya kepada personel militer atau petugas kesehatan yang bekerja pada garis depan. Jadi, tidak diberikan kepada masyarakat umum. Itu pun dengan catatan, jika ditemukan defisiensi atau efek samping serius, persetujuan vaksin akan dicabut kembali.
Keempat, walau membuka pintu EUA untuk vaksin Covid-19, regulatory body berbagai negara menerapkan prinsip yang cukup ketat. Di Amerika, FDA menyebut EUA bagi vaksin Covid-19 sebagai EUA-plus, yang kriterianya lebih ketat dibandingkan dengan EUA produk medis lain. Di antaranya, vaksin harus memiliki paling tidak 2 bulan follow-up setelah dosis kedua diberikan pada fase 3 serta harus memiliki efikasi minimal 50 persen. Dengan kriteria yang ketat tersebut, tidak mudah sebuah vaksin Covid-19 memperoleh EUA.
Persetujuan penggunaan vaksin lewat EUA memang merupakan salah satu alternatif dalam masa krisis. Namun, opsi ini memiliki risiko kesehatan dan keselamatan yang signifikan.

Iqbal Mochtar
Pemerintah harus berpikir jernih sebelum memutuskan apakah akan menggunakan vaksin lewat jalur cepat EUA dengan segala risikonya atau menunda program vaksin beberapa bulan dengan risiko yang lebih minimal dan terkontrol.
Iqbal Mochtar, Dokter dan Pemerhati Masalah Kesehatan